Kalp kapaklarının doku mühendisliği - Tissue engineering of heart valves
Doku mühendisliği kalp kapakçıkları (TEHV) Tam veya kısmi bir kalbe ihtiyacı olan insanlar için yaşayan bir kalp kapağı oluşturmaya yönelik yeni ve ilerleyen bir önerilen tedavi önerin valf değişimi. Şu anda, yılda çeyrek milyondan fazla protez kalp kapağı implante edilmektedir.[1] ve replasman ameliyatı gerektiren hastaların sayısının önümüzdeki elli yıl içinde artacağından ve hatta üç katına çıkacağından şüpheleniliyor.[2] Gibi sunulan mevcut tedaviler mekanik valfler veya biyolojik valfler kişinin sağlığına zararlı değildir, biyolojik kapaklar yapısal bozulmaya ve yeniden çalışmaya duyarlıyken mekanik kapaklar ömür boyu antikoagülan kullanımını gerektirdiğinden her ikisinin de kendi sınırlamaları vardır.[2][3] Böylece, yerinde (orijinal konumunda veya yerinde) kalp kapakçıklarının doku mühendisliği, insan vücudunun biyolojik sistemi içinde büyüyebilen, adapte olabilen ve etkileşime girebilen, konakçının kendi hücrelerinden oluşan canlı bir kalp kapağı yaratma kullanımını araştıran yeni bir yaklaşım olarak hizmet eder.[4]
Araştırma henüz klinik araştırma aşamasına gelmemiştir.
Prosedür
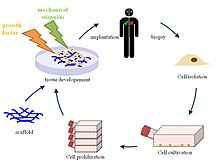
İskeleler
Çeşitli biyomalzemeler İster biyolojik, ister sentetik veya her ikisinin bir kombinasyonu olsun, bir insan vücuduna implante edildiğinde konağı destekleyebilen iskeleler oluşturmak için kullanılabilir. doku yenilenmesi.[5] Öncelikle iskelenin implante edileceği hastanın hücreleri toplanır. Bu hücreler, oluşturulan iskeleye genişletilir ve tohumlanır ve daha sonra insan vücuduna yerleştirilir.[6] İnsan vücudu bir biyoreaktör görevi görür ve bu da bir hücre dışı matris (ECM) kalp için gerekli ortamı sağlamak için iskele etrafındaki lifli proteinlerle birlikte ve kan dolaşım sistemi.[7] Yabancı iskelenin ilk implantasyonu, kılavuzluk eden çeşitli sinyal yollarını tetikler. yabancı cisim yanıtı komşu dokulardan hücre alımı için.[2] İskeleyi çevreleyen yeni nanofiber ağ, ana gövdenin doğal ECM'sini taklit eder.[8] Hücreler hücreyi doldurmaya başladığında, yapı iskelesi yavaş yavaş bozunacak şekilde tasarlanır ve geride konakçı vücudun kendi hücrelerinden yapılmış, hücre repopülasyonunu tamamen yapabilen ve vücuttaki çevresel değişikliklere tam olarak dayanabilen yapılandırılmış bir kalp kapakçığı bırakır.[9] Doku mühendisliği için tasarlanan iskele en önemli bileşenlerden biridir çünkü implantasyon ve bozulmadan çok sonra doku yapımına, canlılığa ve işlevselliğe rehberlik eder.
Biyolojik

Biyolojik iskeleler, insan donör dokusundan veya hayvanlardan oluşturulabilir; bununla birlikte, hayvan dokusu daha yaygın olarak erişilebilir ve daha bol olduğu için genellikle daha popülerdir.[10] Ksenograft alıcıdan farklı bir türden bir donörden kalp kapakçıkları domuzlardan, ineklerden veya koyunlardan olabilir.[8] İnsan veya hayvan dokusu kullanılıyorsa, yararlı iskeleler oluşturmanın ilk adımı hücresizleştirme ECM matrisini korurken hücresel içeriği tamamen kaldırmak anlamına gelir,[11] sıfırdan sentetik iskele üretmeye göre avantajlıdır. Hücresel malzeme etkileşimlerini bozan noniyonik ve iyonik deterjanların kullanımı veya peptit bağlarını, RNA'yı ve DNA'yı ayırmak için enzimlerin kullanımı gibi birçok hücresizleştirme yöntemi kullanılmıştır.[8]
Fabrikasyon
Ayrıca iskeleler üreten ve bunları biyolojik ipuçlarıyla birleştiren güncel yaklaşımlar da vardır.[2] Fabrikasyon iskeleler, görüntüleme teknikleri kullanılarak gözlemlenen doğal kalp kapakçığını taklit etmek için biyolojik, sentetik veya her iki malzemenin bir kombinasyonu kullanılarak da üretilebilir. İskele ham maddelerden oluşturulduğundan, iskelenin özelliklerini kontrol etmede çok daha fazla esneklik vardır ve daha uygun hale getirilebilir. Bazı fabrikasyon yapı iskeleleri türleri, hücresel döküntülerin içinden akışına izin vererek daha fazla doku ve damar büyümesine izin veren geniş bir gözenek ağına sahip katı 3-D gözenekli iskeleleri içerir.[12] 3-D gözenekli iskeleler, 3-D baskı veya poliglikolik asit (PGA) ve polilaktik asitten (PLA) kolajen gibi daha doğal polimerlere kadar çeşitli polimerlerle üretilebilir.[8]
Lifli yapı iskeleleri, yüksek ısıya sahip lifler sayesinde ECM'nin yapısını yakından eşleştirme potansiyeline sahiptir. Büyüme faktörü. Lifli iskeleler üretme teknikleri şunları içerir: Elektrospinning,[13][11] ince lifler üretmek için uygulanan yüksek elektrik voltajından sıvı bir polimer çözeltisinin gerildiği. 3-D gözenekli iskelelerin tersine, lifli iskeleler, iskeledeki hücrelerin yayılmasını önleyen çok küçük bir gözenek boyutuna sahiptir.[14]
Hidrojel iskeleler, hidrofilik polimerlerin çeşitli reaksiyonlarla çapraz bağlanmasıyla oluşturulur. serbest radikal polimerizasyonu veya eşlenik ekleme reaksiyonu.[8] Hidrojeller faydalıdır çünkü yüksek su içeriğine sahiptirler, bu da besinlerin ve küçük malzemelerin kolay geçişine izin verir.[15]
Biyouyumluluk
biyouyumluluk Cerrahi olarak implante edilmiş yabancı biyomateryal, biyomateryal ve konakçı vücut dokusu arasındaki etkileşimleri ifade eder. Hücre hattı ve hücre tipi gibi fibroblastlar hücre morfolojisini değiştirerek implante edilmiş yabancı cihazlara yönelik doku tepkilerini büyük ölçüde etkileyebilir.[16] Böylece hücre kaynağı yanı sıra protein adsorpsiyonu Biyomateryal yüzey özelliğine bağlı olan, iskele bölgesinde doku tepkisi ve hücre infiltrasyonunda önemli bir rol oynar.
Metodoloji
Tahrik edici cevap
Akut inflamasyon
Ameliyat yoluyla herhangi bir yabancı cihaz veya materyalin implantasyonu, en azından bir dereceye kadar doku travmasına neden olur. Bu nedenle, özellikle doğal bir kalp kapakçığını kısmen veya tamamen çıkarırken, doku travması bir dizi inflamatuar yanıtları tetikleyecek ve akut inflamasyon. Akut iltihabın ilk aşamasında, vazodilasyon büyüme faktörlerinin, sitokinlerin ve diğer bağışıklık hücrelerinin salınmasıyla birlikte yara bölgesine kan akışını arttırır. Ayrıca hücreler, çevreleyen dokuda ikincil hasara neden olan reaktif oksijen türlerini ve sitokinleri serbest bırakır.[17] Bu kimyasal faktörler daha sonra monositler veya beyaz kan hücreleri gibi diğer bağışıklığa yanıt veren hücrelerin toplanmasını teşvik eder ve bu da bir kan pıhtısı ve protein açısından zengin matris oluşumunu teşvik etmeye yardımcı olur.
Kronik iltihap
Akut enflamatuar yanıt devam ederse, vücut daha sonra geçmeye başlar. kronik iltihap. Bu sürekli ve sistemik iltihaplanma aşamasında, birincil itici güçlerden biri sızıntıdır. makrofajlar. Makrofajlar ve lenfositler, biyomateryal bölgeye besin sağlamaya yardımcı olmak için yeni dokuların ve kan damarlarının oluşumunu tetikler. Yeni fibröz doku daha sonra biyomateryal ve çevreleyen doku arasındaki etkileşimleri en aza indirmek için yabancı biyomateryali kapsül içine alır. Kronik inflamasyonun uzaması bir enfeksiyon için olası bir gösterge olabilirken, bazen inflamasyon ameliyattan sonra beş yıla kadar mevcut olabilir. Bir cihazın implantasyonundan 30 gün sonra sıçan hücrelerinde fibroz ve enflamatuar hücrelerin varlığı ile belirgin kronik enflamasyon gözlendi.[18]
Kronik inflamasyonu takiben, hücresel artıkların birikmesi nedeniyle implantasyondan yaklaşık 60 gün sonra mineralizasyon meydana gelir ve kireçlenme in vivo olarak biyo-uyumlu implante cihazların işlevselliğini tehlikeye atma potansiyeline sahip.

Yabancı cisim tepkisi
Normal fizyolojik koşullar altında, enflamatuar hücreler vücudu yabancı cisimlerden korur ve vücut bir yabancı cisim reaksiyonu biyomateryal yüzeyde kan ve proteinlerin adsorpsiyonuna dayanır. İmplant sonrası ilk iki ila dört hafta içinde, biyomateryal yapışık makrofajlar ile yabancı implant bölgesinin yakınında sitokin ekspresyonu arasında bir ilişki vardır ve bu, kullanılarak keşfedilebilir. yarı kantitatif RT-PCR.[19] Makrofajlar birleşerek oluşur yabancı cisim dev hücreleri (FBGC'ler), benzer şekilde hücre zarlarında sitokin reseptörlerini eksprese eder ve enflamatuar yanıta aktif olarak katılır. Silikon kauçuğa kıyasla organik polieter poliüretan (PEU) kalp pillerinde cihaz arızası, yabancı cisim tepkisinin gerçekten de biyomateryallerin bozulmasına yol açarak daha sonra cihaz arızalarına neden olabileceğini göstermektedir. Biyomateryal bozulma oranını en aza indirmek ve yavaşlatmak için işlevsellik ve dayanıklılıktan ödün verilmesini önlemek için kullanılması önerilmektedir.[19]
Faydaları
Doku mühendisliği yapılmış kalp kapakçıkları, geleneksel biyolojik ve mekanik valflere göre belirli avantajlar sunar:
- Canlı kapakçık - Canlı kapakçık büyüme ve biyolojik ortamına tepki verme yeteneğine sahip olduğundan, canlı kalp kapakçığı değiştirme seçeneği çocuklar için oldukça uygundur, bu özellikle vücutları sürekli değişen çocuklar için yararlıdır.[11] Bu seçenek, bir çocuğun hayatında ihtiyaç duyulan yeniden ameliyat sayısını azaltmaya yardımcı olacaktır.
- Özelleştirilmiş süreç - Doku mühendisliğinde kullanılan iskeleler sıfırdan üretilebildiğinden, daha yüksek derecede esneklik ve kontrol vardır. Bu, doku mühendisliği ile tasarlanmış kalp kapakçıkları ve iskelenin şekli ve biyomateryal yapısı gibi özelliklerinin özel olarak hastaya göre uyarlanmasına olanak tanır.
Riskler ve zorluklar

Doku mühendisliği yapılmış kalp kapakçıkları klinik olarak tam olarak uygulanmadan önce birçok risk ve zorluk hala ele alınmalı ve araştırılmalıdır:
- Kontaminasyon - Belirli kaynak materyaller, virüslerin ve bulaşıcı hastalıkların duyarlılığına elverişli bir mikrobiyolojik ortamı teşvik edebilir.[20] İnsan vücuduna harici bir iskele yerleştirildiğinde, kirlenme kaçınılmaz olsa da, steril tekniğin uygulanmasıyla azaltılabilir.
- İskele Etkileşimleri - Spesifik biyouyumluluk gereksinimleri mevcut araştırmalarla hala büyük ölçüde bilinmediğinden, hücreler ve implante edilen iskele arasındaki etkileşimlerle ilişkili birçok risk vardır.[20] Bu etkileşimlere verilen yanıt da oldukça bireyseldir ve spesifik hastanın biyolojik ortamına bağlıdır; bu nedenle, daha önce araştırılan hayvan modelleri, insan vücudundaki sonuçları doğru bir şekilde gösteremeyebilir.[21] Yapı iskelesi ve çevreleyen doku arasındaki son derece etkileşimli yapı nedeniyle, biyobozunurluk, biyouyumluluk ve immünojenite gibi özelliklerin tümü, nihai ürünün performansında anahtar faktörler olduğundan dikkatlice düşünülmelidir.[20][11]
- Yapısal karmaşıklık - Heterojen yapılarıyla kalp kapakçıkları çok karmaşık ve dinamiktir,[21] bu nedenle doku mühendisliği yapılmış kapakçıkların taklit etmesi zor. Yeni kapaklar, doğal kapağın anatomik şeklini ve mekanik işlevlerini karşılarken aynı zamanda yüksek dayanıklılığa sahip olmalıdır.[11]
Tarih
Sentetik iskeleler
Çeşitli hücre hatlarına sahip polimerlerden yapılmış tohumlanmış iskelelerde yapılan çalışmalar laboratuvar ortamındayapı iskelelerinin zamanla bozulduğu ve geride hücresel bir matris ve proteinler bıraktığı. Kalp kapaklarının doku mühendisliği üzerine ilk çalışma 1995 yılında yayınlandı.[11] 1995 ve 1996 yıllarında Shinoka, insan implantasyonu için FDA tarafından onaylanan poliglikolik asitten (PGA) yapılmış bir yapı iskelesi kullandı ve koyunun pulmoner kapak broşürünü değiştirmek amacıyla koyun endotel hücreleri ve fibroblastlar ile tohumladı.[22] Shinoka'nın çalışmasının sonucu, çok daha kalın ve daha sert olan tasarlanmış bir kalp kapakçığıydı; bu, Hoerstrup'u bir poli-4-hidroksibütirat (P4HB) kaplı PGA iskelesi ve koyun kullanarak bir koyundaki üç pulmoner kapak broşürünün tümünü değiştirmek için bir çalışma yürütmesini sağladı. endotelyal hücreler ve miyofibroblast.[23]
Biyolojik iskeleler
Üzerinde çalışılan bir başka seçenek de hücresizleştirilmiş biyolojik yapı iskeleleri kullanmak ve bunları karşılık gelen hücrelerle tohumlamaktı. laboratuvar ortamında.[21] 2000 yılında Steinhoff, koyun endotel hücreleri ve miyofibroblastlar ile tohumlanan hücresizleştirilmiş bir koyun pulmoner kapak iskelesi implante etti.[24] Dohmen daha sonra hücresizleştirilmiş bir kriyoprezerve pulmoner allogreft iskele oluşturdu ve 2002'de bir insan hastada sağ ventriküler çıkış yolunu (RVOT) yeniden yapılandırmak için insan vasküler endotelyal hücreleri ile tohumladı.[25] Perry, 2003 yılında koyun mezenkimal kök hücreleri ile P4HB kaplı PGA iskelesi tohumladı laboratuvar ortamında; ancak, bir in vivo çalışma yapılmadı.[26] 2004 yılında Iwai, bir köpeğin pulmoner arterinin yerinde endotelyal ve düz kas hücreleri ile tohumlanan kolajen mikro sünger küre iskelesi ile birleştirilmiş bir poli (laktik-ko-glikolik asit) PLGA kullanarak bir çalışma yürüttü.[27] 2005 yılında Sutherland, bir koyundaki üç pulmoner kapak broşürünün tümünü değiştirmek için PGA tohumlu koyun mezenkimal kök hücre ve poli-L-laktik asit (PLLA) iskelesi kullandı.[28]
İn vivo implant çalışmaları
Bir avuç çalışma, kalp kapakçıklarının doku mühendisliğini kullandı in vivo hayvan modellerinde ve insanlarda. 2000 yılında Matheny, bir pulmoner kapak broşürünü değiştirmek için bir domuzun ince bağırsak submukozasını kullandığı bir çalışma yürüttü.[29] Klinik bir ortamda da sınırlı çalışmalar yapılmıştır. Örneğin 2001 yılında Elkins, SynerGraft ile tedavi edilen hücresizleştirilmiş insan pulmoner kapaklarını hastalara implante etti.[30] Simon benzer şekilde çocuklarda implantasyon için SynerGraft hücresizleştirilmiş domuz kapakçıkları kullandı;[31] bununla birlikte, bu valfler, konakçı hücreler olmadığından, bunun yerine iskele bölgesinde bulunan yüksek miktarlarda enflamatuar hücreler olduğundan büyük ölçüde başarısız oldu.[32][33][8] Dohmen, Konertz ve Almanya'nın Berlin kentindeki meslektaşları tarafından yürütülen çalışmalar, ameliyat geçiren 50 hastada biyolojik bir domuz kapağı implantasyonunu içeriyordu. Ross operasyonu 2002'den 2004'e kadar.[33] Ortanca yaşı 46 olan yetişkinlerde, matrix P olarak da adlandırılan hücresizleştirilmiş domuz ksenogreft kapakçığı kullanılarak çalışmanın amacı, pulmoner kapak replasmanı için bir öneri sunmaktı. Bazı hastalar ameliyat sonrası öldü ve yeniden ameliyata girmek zorunda kalırken, kapak doğal, sağlıklı bir kapağa benzer şekilde davrandığı için kısa vadeli sonuçlar iyi gidiyor gibi görünüyor.[34] Bir hayvan denemesi, transkateter aort kapak değişimi Doku mühendisliği yapılmış kalp kapakçıkları (TEHV'ler) ile (TAVR) prosedürü. İnsan hücresinden türetilmiş hücre dışı matriks ile entegre edilmiş bir TAVR stenti koyunlara implante edildi ve incelendi; burada kapak yapısal bütünlüğü ve hücre infiltrasyonunu korudu ve potansiyel klinik uygulamanın TAVR'yi daha genç hastalara yaymasına izin verdi.[35]
Araştırma
Birçok iken in vitro ve in vivo hayvan modellerinde test edilmiş, hayvan modellerinden insanlara çeviri henüz başlamamıştır. Cerrahi kesi yerlerinin boyutu, prosedürün süresi ve mevcut kaynaklar ve maliyet gibi faktörlerin tümü dikkate alınmalıdır.[36] Sentetik nanomalzemeler, kalp kapakçıklarının doku mühendisliğinde kullanılan iskeleleri geliştirme potansiyeline sahiptir. Kullanımı nanoteknoloji daha yüksek gerilme mukavemeti gibi imal edilmiş iskelelerin faydalı özelliklerinin genişletilmesine yardımcı olabilir.[37]
Ayrıca bakınız
Referanslar
- ^ Jegatheeswaran A, Butany J (2006). "Protez kalp kapakçıklarında bulaşıcı ve iltihaplı hastalıkların patolojisi". Kardiyovasküler Patoloji. 15 (5): 252–255. doi:10.1016 / j.carpath.2006.05.002. PMID 16979031.
- ^ a b c d Mol A, Smits AI, Bouten CV, Baaijens FP (Mayıs 2009). "Kalp kapakçıklarının doku mühendisliği: gelişmeler ve mevcut zorluklar". Tıbbi Cihazların Uzman Değerlendirmesi. 6 (3): 259–75. doi:10.1586 / erd.09.12. PMID 19419284.
- ^ Goldsmith I, Turpie AG, Lip GY (Kasım 2002). "Valvar kalp hastalığı ve protez kalp kapakları". BMJ. 325 (7374): 1228–31. doi:10.1136 / bmj.325.7374.1228. PMC 1124694. PMID 12446543.
- ^ Bouten CV, Smits AI, Baaijens FP (2018-05-29). "Kalbin İçinde Valfler Yetiştirebilir miyiz? Malzeme Bazlı Yerinde Kalp Kapağı Doku Mühendisliği Perspektifi". Kardiyovasküler Tıpta Sınırlar. 5: 54. doi:10.3389 / fcvm.2018.00054. PMC 5987128. PMID 29896481.
- ^ "Doku mühendisliği için biyomalzemeler ve iskeleler". Günümüz Malzemeleri. 14 (3): 88–95. 2011-03-01. doi:10.1016 / S1369-7021 (11) 70058-X. ISSN 1369-7021.
- ^ Schmidt D, Stock UA, Hoerstrup SP (Ağustos 2007). "Hücresizleştirilmiş ksenojenik veya polimerik starter matrisleri kullanarak kalp kapakçıklarının doku mühendisliği". Londra Kraliyet Cemiyeti'nin Felsefi İşlemleri. Seri B, Biyolojik Bilimler. 362 (1484): 1505–12. doi:10.1098 / rstb.2007.2131. PMC 2440411. PMID 17588875.
- ^ Gandaglia A, Bagno A, Naso F, Spina M, Gerosa G (Nisan 2011). "Doku mühendisliği yapılmış kalp kapakçıkları için hücreler, iskeleler ve biyoreaktörler: temel kavramlardan çağdaş gelişimsel yeniliklere bir yolculuk". Avrupa Kardiyo-Göğüs Cerrahisi Dergisi. 39 (4): 523–31. doi:10.1016 / j.ejcts.2010.07.030. PMID 21163670.
- ^ a b c d e f Jana S, Tefft BJ, Spoon DB, Simari RD (Temmuz 2014). "Kalp kapaklarının doku mühendisliği için iskeleler". Acta Biomaterialia. 10 (7): 2877–93. doi:10.1016 / j.actbio.2014.03.014. PMID 24675108.
- ^ Xue Y, Sant V, Phillippi J, Sant S (Ocak 2017). "Doku mühendisliği yapılmış kalp kapakçıkları için biyolojik olarak parçalanabilir ve biyomimetik elastomerik iskeleler". Acta Biomaterialia. 48: 2–19. doi:10.1016 / j.actbio.2016.10.032. PMID 27780764.
- ^ Alrefai MT, Murali D, Paul A, Ridwan KM, Connell JM, Shum-Tim D (2015-05-14). "Hücre bazlı tedavi kullanarak kalp dokusu mühendisliği ve rejenerasyonu". Kök Hücreler ve Klonlama: Gelişmeler ve Uygulamalar. 8: 81–101. doi:10.2147 / SCCAA.S54204. PMC 4437607. PMID 25999743.
- ^ a b c d e f Cheung DY, Duan B, Kasap JT (2015). "Kalp kapakçıklarının doku mühendisliğinde güncel ilerleme: çok ölçekli sorunlar, çok ölçekli çözümler". Biyolojik Terapi Konusunda Uzman Görüşü. 15 (8): 1155–72. doi:10.1517/14712598.2015.1051527. PMC 4883659. PMID 26027436.
- ^ Loh QL, Choong C (Aralık 2013). "Doku mühendisliği uygulamaları için üç boyutlu iskeleler: gözeneklilik ve gözenek boyutunun rolü". Doku Mühendisliği Bölüm B: İncelemeler. 19 (6): 485–502. doi:10.1089 / ten.teb.2012.0437. PMC 3826579. PMID 23672709.
- ^ brahim DM, Kakarougkas A, Allam NK (2017). "Doku mühendisliği yapılmış kalp kapakçıkları için matrisler olarak elektrospun iskelelerdeki son gelişmeler". Günümüzde Malzemeler Kimya. 5: 11–23. doi:10.1016 / j.mtchem.2017.05.001. ISSN 2468-5194.
- ^ Bružauskaitė I, Bironaitė D, Bagdonas E, Bernotienė E (Mayıs 2016). "Doku rejenerasyonu için iskeleler ve hücreler: farklı yapı iskelesi gözenek boyutları - farklı hücre etkileri". Sitoteknoloji. 68 (3): 355–69. doi:10.1007 / s10616-015-9895-4. PMC 4846637. PMID 26091616.
- ^ Zhu J, Marchant RE (Eylül 2011). "Hidrojel doku mühendisliği iskelelerinin tasarım özellikleri". Tıbbi Cihazların Uzman Değerlendirmesi. 8 (5): 607–26. doi:10.1586 / erd.11.27. PMC 3206299. PMID 22026626.
- ^ Morais JM, Papadimitrakopoulos F, Burgess DJ (Haziran 2010). "Biyomalzemeler / doku etkileşimleri: yabancı cisim tepkisinin üstesinden gelmek için olası çözümler". AAPS Dergisi. 12 (2): 188–96. doi:10.1208 / s12248-010-9175-3. PMC 2844517. PMID 20143194.
- ^ Mittal, Manish; Siddiqui, Mohammad Rizwan; Tran, Khiem; Reddy, Sekhar P .; Malik, Asrar B. (2014-03-01). "Enflamasyonda ve Doku Hasarında Reaktif Oksijen Türleri". Antioksidanlar ve Redoks Sinyali. 20 (7): 1126–1167. doi:10.1089 / ars.2012.5149. ISSN 1523-0864. PMC 3929010. PMID 23991888.
- ^ Onuki Y, Bhardwaj U, Papadimitrakopoulos F, Burgess DJ (Kasım 2008). "İmplante edilebilir cihazların biyouyumluluğunun bir incelemesi: yabancı cisim yanıtının üstesinden gelmek için mevcut zorluklar". Diyabet Bilim ve Teknoloji Dergisi. 2 (6): 1003–15. doi:10.1177/193229680800200610. PMC 2769826. PMID 19885290.
- ^ a b Anderson JM, Rodriguez A, Chang DT (Nisan 2008). "Biyomalzemelere yabancı cisim reaksiyonu". İmmünolojide Seminerler. 20 (2): 86–100. doi:10.1016 / j.smim.2007.11.004. PMC 2327202. PMID 18162407.
- ^ a b c Williams D (Mayıs 2004). "Doku mühendisliğinde fayda ve risk". Günümüz Malzemeleri. 7 (5): 24–29. doi:10.1016 / s1369-7021 (04) 00232-9.
- ^ a b c Mendelson K, Schoen FJ (Aralık 2006). "Kalp kapağı doku mühendisliği: kavramlar, yaklaşımlar, ilerleme ve zorluklar". Biyomedikal Mühendisliği Yıllıkları. 34 (12): 1799–819. doi:10.1007 / s10439-006-9163-z. PMC 1705506. PMID 17053986.
- ^ Shinoka T, Breuer CK, Tanel RE, Zund G, Miura T, Ma PX, Langer R, Vacanti JP, Mayer JE (Aralık 1995). "Doku mühendisliği kalp kapakçıkları: kuzu modelinde kapakçık değiştirme çalışması". Göğüs Cerrahisi Yıllıkları. 60 (6 Ek): S513-6. doi:10.1016/0003-4975(95)00733-4. PMID 8604922.
- ^ Hoerstrup SP, Sodian R, Daebritz S, Wang J, Bacha EA, Martin DP, Moran AM, Guleserian KJ, Sperling JS, Kaushal S, Vacanti JP, Schoen FJ, Mayer JE (Kasım 2000). "In vitro büyütülmüş fonksiyonel canlı trileaflet kalp kapakçıkları". Dolaşım. 102 (19 Ek 3): III44-9. doi:10.1161 / 01.cir.102.suppl_3.iii-44. PMID 11082361.
- ^ Steinhoff G, Stock U, Karim N, Mertsching H, Timke A, Meliss RR, Pethig K, Haverich A, Bader A (Kasım 2000). "Allojenik aselüler matriks kanalları üzerinde pulmoner kalp kapaklarının doku mühendisliği: kapak dokusunun in vivo restorasyonu". Dolaşım. 102 (19 Özel Sayı 3): III50-5. doi:10.1161 / 01.cir.102.suppl_3.iii-50. PMID 11082362.
- ^ Dohmen PM, Costa F, Lopes SV, Yoshi S, Souza FP, Vilani R, Costa MB, Konertz W (2005-03-09). "Juvenil koyun modeline implante edilen hücresizleştirilmiş domuz kalp kapakçığının sonuçları". Kalp Cerrahisi Forumu. 8 (2): E100–4, tartışma E104. doi:10.1532 / hsf98.20041140. PMID 15769723.
- ^ Perry TE, Kaushal S, Sutherland FW, Guleserian KJ, Bischoff J, Sacks M, Mayer JE (Mart 2003). "Göğüs Cerrahisi Yöneticileri Derneği Ödülü. Doku mühendisliği kalp kapakçıkları için bir hücre kaynağı olarak kemik iliği". Göğüs Cerrahisi Yıllıkları. 75 (3): 761–7, tartışma 767. doi:10.1016 / S0003-4975 (02) 03776-1. PMID 12645690.
- ^ Iwai S, Sawa Y, Ichikawa H, Taketani S, Uchimura E, Chen G, Hara M, Miyake J, Matsuda H (Eylül 2004). "Kolajen mikro süngerli biyolojik olarak parçalanabilir polimer, yeni bir biyomühendislik kardiyovasküler protez görevi görür". Göğüs Kalp Damar Cerrahisi Dergisi. 128 (3): 472–9. doi:10.1016 / j.jtcvs.2004.04.013. PMID 15354111.
- ^ Sutherland FW, Perry TE, Yu Y, Sherwood MC, Rabkin E, Masuda Y, Garcia GA, McLellan DL, Engelmayr GC, Sacks MS, Schoen FJ, Mayer JE (Mayıs 2005). "Kök hücrelerden canlı otolog yarım ay kalp kapakçığına". Dolaşım. 111 (21): 2783–91. doi:10.1161 / SİRKÜLASYONAHA.104.498378. PMID 15927990.
- ^ Matheny RG, Hutchison ML, Dryden PE, Hiles MD, Shaar CJ (Kasım 2000). "Bir pulmoner kapak yaprakçık ikamesi olarak domuz ince bağırsak submukozası". Kalp Kapakçığı Hastalığı Dergisi. 9 (6): 769–74, tartışma 774–5. PMID 11128782.
- ^ Elkins RC, Dawson PE, Goldstein S, Walsh SP, Black KS (Mayıs 2001). "Hücresizleştirilmiş insan kapak allogreftleri". Göğüs Cerrahisi Yıllıkları. 71 (5 Ek): S428-32. doi:10.1016 / S0003-4975 (01) 02503-6. PMID 11388241.
- ^ Simon P, Kasimir MT, Seebacher G, Weigel G, Ullrich R, Salzer-Muhar U, Rieder E, Wolner E (Haziran 2003). "Pediyatrik hastalarda doku mühendisliği yapılmış domuz kalp kapağı SYNERGRAFT'ın erken başarısızlığı". Avrupa Kardiyo-Göğüs Cerrahisi Dergisi. 23 (6): 1002–6, tartışma 1006. doi:10.1016 / S1010-7940 (03) 00094-0. PMID 12829079.
- ^ Sayk F, Bos I, Schubert U, Wedel T, Sievers HH (Mayıs 2005). "Yeni bir hücresizleştirilmiş pulmoner homograftta histopatolojik bulgular: bir otopsi çalışması". Göğüs Cerrahisi Yıllıkları. 79 (5): 1755–8. doi:10.1016 / j.athoracsur.2003.11.049. PMID 15854972.
- ^ a b Vesely I (Ekim 2005). "Kalp kapakçığı doku mühendisliği". Dolaşım Araştırması. 97 (8): 743–55. doi:10.1161 / 01.RES.0000185326.04010.9f. PMID 16224074.
- ^ Konertz W, Dohmen PM, Liu J, Beholz S, Dushe S, Posner S, Lembcke A, Erdbrügger W (Ocak 2005). Ross operasyonu sırasında pulmoner kapak replasmanı için Matrix P hücresizleştirilmiş ksenogreftin hemodinamik özellikleri ". Kalp Kapakçığı Hastalığı Dergisi. 14 (1): 78–81. PMID 15700440.
- ^ Lintas V, Fioretta ES, Motta SE, Dijkman PE, Pensalfini M, Mazza E, Caliskan E, Rodriguez H, Lipiski M, Sauer M, Cesarovic N, Hoerstrup SP, Emmert MY (Aralık 2018). "Transkateter Aort Kapakçık Değişimi için İnsan Hücresinden Tissue-Engineered Yeni Bir Kalp Kapakçığının Geliştirilmesi: In Vitro ve In Vivo Fizibilite Çalışması". Kardiyovasküler Çeviri Araştırmaları Dergisi. 11 (6): 470–482. doi:10.1007 / s12265-018-9821-1. PMID 30105605.
- ^ Shinoka T, Miyachi H (Kasım 2016). "Doku Mühendisliği Kalp Kapağının Mevcut Durumu". Dünya Pediatrik ve Konjenital Kalp Cerrahisi Dergisi. 7 (6): 677–684. doi:10.1177/2150135116664873. PMID 27834758.
- ^ Rippel RA, Ghanbari H, Seifalian AM (Temmuz 2012). "Doku mühendisliği kalp kapağı: kalp cerrahisinin geleceği". Dünya Cerrahi Dergisi. 36 (7): 1581–91. doi:10.1007 / s00268-012-1535-y. PMID 22395345.
